不同OCT分型的糖尿病性黄斑水肿与血小板参数的关系
摘要:目的 研究不同OCT分型的糖尿病性黄斑水肿(diabetic macular edema,DME)与血小板参数的关系。方法 回顾性研究。118例(118眼)糖尿病视网膜病变(diabetic retinopathy,DR)患者中,DME组88眼,未合并DME(Non-DME)组30眼,根据DME的OCT形态分为弥漫性视网膜增厚型(diffuse retinal thickening,DRT)27眼、黄斑囊样水肿(cystoid macular edema,CME)29眼、神经上皮层脱离型(neurosensory retinal detachment,NSD)32眼,对不同组别间患者血小板计数(platelet count,PLT)、平均血小板体积(mean platelet volume,MPV)、血小板平均分布宽度(platelet distribution width,PDW)和血小板压积(plateletcrit,PCT)进行比较,并分析DR分期与DME的OCT分型间的关系。结果 DRT在轻度和中度非增生型DR中的占比为50.0%,而NSD在重度非增生型DR及增生型DR患眼中的占比较高,为84.5%。DME组患者的MPV和PDW均明显高于Non-DME组(均为P<0.05),NSD患者的MPV和PDW均明显高于DRT和CME患者(均为P<0.05)。结论 不同DME分型的患者MPV、PDW有差异,血小板与NSD的发生、发展可能相关。
关键词:糖尿病性黄斑水肿; OCT; 平均血小板体积; 血小板平均分布宽度;
当前,糖尿病性黄斑水肿(diabetic macular edema,DME)已成为糖尿病患者视力损失的主要原因[1],DME的病因主要为多因素导致的血-视网膜屏障的破坏,使视网膜内及视网膜下的液体积聚,但详细的发病过程及病理机制仍处于研究中。
相关研究发现,平均血小板体积(mean platelet volume,MPV)、血小板平均分布宽度(platelet distribution width,PDW)和血小板压积(plateletcrit,PCT)等的升高与糖尿病、冠心病等疾病的发生、发展密切相关[2-3]。糖尿病患者由于长期处于高糖状态,糖代谢紊乱,可引起慢性炎症、内皮细胞功能紊乱、高凝状态等,从而诱导血小板的活化,导致血小板黏附、聚集、释放等功能增强[4]。而DME的发生、发展与炎症、氧化应激、内皮细胞功能紊乱、血管内皮生长因子的上调等相关[5],且相关研究发现,血小板中可分离出血管内皮生长因子(vascular endothelial growth factor,VEGF)的同源生长因子——血小板源性生长因子(platelet-derived growth factor,PDGF),在糖尿病视网膜病变(diabetic retinopathy,DR)患者玻璃体内PDGF表达增加[6],因此推测,DME与血小板可能存在一定相关性。Tetikogˇlu等[7]及李海东等[8]通过研究MPV与2型糖尿病患者的不同DR分期及DME的关系,从而推测较高的MPV可能为DME发生、发展的危险因素。Kang等[9]研究表明,不同OCT分型的DME形态特征及病理机制均不同,根据DME的不同OCT形态进行分型对DME的诊断和治疗具有重要的价值。本研究在验证Tetikogˇlu等[7]及李海东等[8]的DME与血小板可能相关的结论后,根据DME的OCT形态进行分组,进一步研究不同OCT分型的DME与血小板的关系。
1 资料与方法
1.1 一般资料
回顾性研究。将2014年9月至2018年9月于南方医科大学珠江医院眼科住院就诊的DR患者118例118眼纳入研究。其中,男65例65眼、女53例53眼,年龄38~80(57.0±8.9)岁。纳入标准:诊断为2型糖尿病且行FFA及OCT检查明确为DR的患者。排除标准:(1)双眼任一眼屈光间质混浊不能清晰观察眼底者;(2)伴有黄斑变性、黄斑前膜、玻璃体黄斑牵拉综合征等眼底疾病者;(3)既往曾行视网膜激光光凝术、玻璃体内注药等治疗及行玻璃体切割等眼内手术者;(4)近期服用波立维、阿司匹林等抗凝、抗血小板药物者;(5)伴有心功能或肾功能不全、脑血管异常、肝功能异常、自身免疫性疾病、感染性疾病、肿瘤等全身情况异常者;(6)孕产妇及患有神经精神疾病不能配合检查者。本研究通过本院伦理委员会批准。
1.2 方法
采集患者的性别、年龄、外周血的血小板参数[包括血小板计数(platelet count,PLT)、MPV、PDW及PCT]。所有患者充分散瞳后行眼底FFA及OCT检查。其中OCT检查使用德国海德堡OCT仪器进行,采用快速扫描,31条水平线对患者双眼进行扫描,叠加成像检查由两位经验丰富的眼科医师独立进行并判断DME分型,排除二者诊断不一致者。根据诊疗指南标准将DR分为轻度非增生型DR(non-proliferative diabetic retinopathy,NPDR)、中度NPDR、重度NPDR、增生型DR(proliferative diabetic retinopathy,PDR)[10]。结合OCT检查并参照文献[9,11-14],对DME的不同OCT形态进行分型:弥漫性视网膜增厚型(diffuse retinal thickening,DRT)、黄斑囊样水肿(cystoid macular edema,CME)、神经上皮层脱离型(neurosensory retinal detachment,NSD)(图1)。3种类型的眼底表现逐渐显着,其中DRT型表现为黄斑区视网膜海绵样肿胀,视网膜内的反射均匀降低;CME表现为黄斑区视网膜可见低反射囊腔,各囊腔间由高反射隔膜分隔;NSD表现为黄斑区视网膜隆起,伴随视网膜色素上皮层的分离,二者间为透明低反射暗腔。若患者双眼DME分型不一致,则选取形态较为显着的一眼纳入研究。若患眼眼底形态存在两种或两种以上类型,则归入表现较为显着的类型,即DRT组:仅DRT;CME组:DRT+CME或仅CME;NSD组为:DRT+CME+NSD或NSD+DRT或DME+NSD或仅NSD。
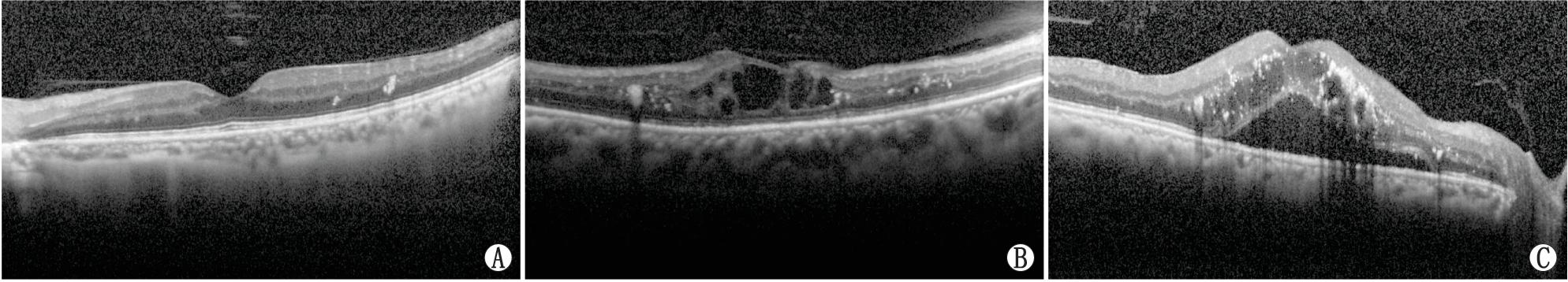
图1 不同分型DME的形态特征
A:DRT;B:CME;C:NSD
1.3 统计学处理
应用SPSS 20.0统计学软件进行数据分析,DME各型的比例与DR分期的关系采用卡方检验及Fisher精确概率检验,对DME与未合并DME(Non-DME)间血小板各参数的比较使用独立样本t检验。DME各分型间的血小板参数比较中,计数资料使用卡方检验,计量资料采用单因素方差分析(one-way ANOVA),两者间的比较采用LSD-t检验。检验水准:α=0.05。
2 结果
2.1 DME与性别的关系
118例患者中,DME组88例,男46例,女42例;Non-DME组30例,男19例,女11例,DME组与Non-DME组之间性别的差异无统计学意义(χ2=1.106,P=0.201)。
2.2 DR分期与DME的关系
118例118眼中,轻度NPDR、中度NPDR、重度NPDR及PDR分别为15眼、19眼、40眼、44眼。其中,在轻度和中度NPDR患者中,DME患者17眼,占50.0%;在重度NPDR及PDR患者中,DME患者71眼,占84.5%。不同DR分期均有DME发生,且随着DR分期的加重,DME的占比增加(χ2=15.215,P<0.001)。
在DME患眼中,DRT、CME、NSD分别为27眼、29眼、32眼。其中,轻度和中度NPDR 17眼DME中,DRT、CME、NSD分别为9眼、6眼、2眼,分别占52.9%、35.3%、11.8%;重度NPDR及PDR 71眼DME中,DRT、CME、NSD分别为18眼、23眼、30眼,分别占25.4%、32.4%、42.3%。在DR不同分期中,各DME分型的占比不同(χ2=6.944,P<0.05),在轻度和中度NPDR患眼中,DRT、CME、NSD的占比逐渐降低;在重度NPDR及PDR患眼中,DRT、CME、NSD的占比逐渐增高。
2.3 DME组与Non-DME组间血小板参数比较
DME组患者的MPV、PDW均显着高于Non-DME组,差异均有统计学意义(均为P=0.000),两组间PLT与PCT相比差异均无统计学意义(均为P>0.05)。见表1。
表1 Non-DME组与DME组的血小板参数
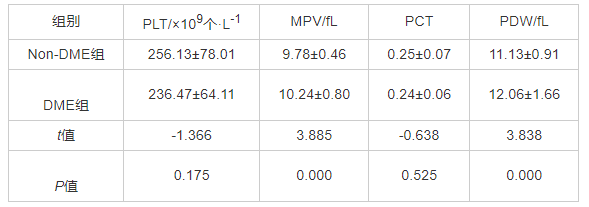
2.4 不同分型的DME与血小板参数的关系
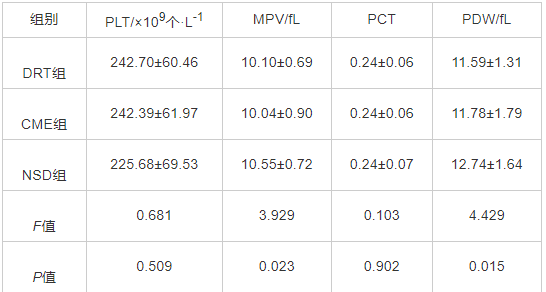
分析不同DME分型患者间的血小板参数,结果显示,DRT组、CME组、NSD组三组间患者的MPV、PDW差异均有统计学意义(均为P<0.05),两两比较结果显示,NSD组患者的MPV、PDW均高于DRT组和CME组(MPV:P=0.029、0.013;PDW:P=0.008、0.023),DRT组与CME组间MPV、PDW相比差异均无统计学意义(P=0.772、0.667)。DRT组、CME组、NSD组间患者的PLT、PCT差异均无统计学意义(均为P>0.05)。见表2。
表2 不同DME分型患者的血小板参数
3 讨论
本研究根据不同的OCT形态特征将DME患眼分为DRT、CME、NSD,结果发现,在不同DR的分期中均有可能出现DME。DME虽然可以发生于DR的任一阶段,但DME在DR不同分期中的占比不同,即DME在重度NPDR及PDR中的占比明显高于轻度和中度NPDR组。在轻度和中度NPDR中,DRT占比最高,重度NPDR及PDR中,NSD占比最高,与Ghosh等[14]、Alkuraya等[15]的研究结果一致,提示DR的分期与DME及DME的不同OCT分型相关。
本研究根据是否存在DME将DR患眼分为Non-DME组与DME组,发现DME组患者的MPV及PDW均显着高于Non-DME组,与Tetikogˇlu等[7]、李海东等[8]的研究结果一致。因此推测,在DR患者中,高MPV值可能是PDR和DME发生的重要危险因素。因在DME的发病机制中,血-视网膜屏障遭到破坏的同时,存在组织缺氧、血流的改变、视网膜局部缺血、炎症等因素。其中炎症作用具有重要意义,包括生长因子表达增加、RPE细胞及视网膜血管内皮细胞功能紊乱、白细胞的黏附、PDGF表达减少、蛋白激酶C的产生等,通过破坏血-视网膜屏障,加剧内皮细胞功能紊乱及血管通透性的增加[5]。而其中血小板活化是血栓形成及炎症疾病病理生理过程中的一个重要环节。活化的血小板在体积增大后可大量产生血小板因子-4、血清素、血小板生长因子等促进血栓形成的物质以发挥其相应的作用[16],因此,MPV的升高提示血小板的功能活跃。且在2型糖尿病患者中,存在多条信号通路紊乱及新陈代谢的异常,例如胰岛素抵抗、高血糖、血脂异常等,均可促进血小板黏附、活化和聚集等,使患者的凝血功能异常增强,血栓形成的几率增加[17]。大量研究也表明,MPV及PDW的升高与糖尿病及其血管性并发症相关[18-19]。同时在DR患者中,低氧等环境诱导可产生生长因子包括VEGF及PDGF,二者为同源性生长因子,最终作用于共同的通路,并可从血小板中分离出PDGF。相关研究也发现,在PDR患者的玻璃体内PDGF明显增高[20-21],因此,结合本研究结果推测,DME组患者的MPV和PDW的升高,可能与血小板的活化有关。
本研究根据OCT的形态特征将DME患眼分为DRT、CME、NSD 3种类型,是由于大量研究表明不同OCT形态下的DME发病机制、治疗方案、治疗效果和预后均存在差异[22-24]。因此,本研究通过验证血小板与DME可能有关,从而进一步研究不同OCT分型的DME与血小板相关参数的关系。其中DRT为缺血导致细胞毒性水肿,出现Müller细胞质肿胀,从而表现为视网膜弥漫的增厚,而且黄斑部海绵样视网膜肿胀主要位于外丛状层。随着前列腺素、VEGF等增加渗透性物质的释放进展为血管源性水肿,持续的水肿或局部缺血使Müller细胞和邻近的神经细胞液化坏死导致囊腔出现,即为CME,囊腔主要出现于内核层及外丛状层。在NSD中,炎症及局部组织缺血使视网膜色素上皮细胞的功能损坏,从脉络膜血管层进入视网膜的液体增加,导致视网膜下液体积聚[9,22]。本研究发现,DRT发生于所有DME患眼中,NSD组患者的MPV及PDW均显着高于DRT组及CME组,CME组与DRT组MPV、PDW差异均无统计学意义。Shimura等[25]研究发现,贝伐单抗在DRT及CME患眼中的疗效较NSD患眼更佳,预后也存在一定差异。结合本研究结果及相关研究我们推测,由于MPV及PDW可反映血小板活化增强,在不同OCT分型的DME患眼中,血小板的活化可能与NSD的发生及发展相关。
本研究为单中心研究,样本量有限,就诊患者有一定区域性且病情多较为严重,因此不能完全代表所有人群的情况;患者的血小板参数可能与全身其他因素相关,例如吸烟等,因此本研究结果可能存在部分偏差;本研究未将男性及女性分开进行分析,不同性别间存在激素等的差异,对结果可能有一定影响;本研究属于横断面研究,不能完全确定其因果关系。综上,仍需要进一步的研究,以更加明确血小板对DME产生的影响,从而为DME的发病机制及治疗的研究提供新的思路。
参考文献
[1] SCHMIDT-ERFURTH U,GARCIA-ARUMI J,BANDELLO F,BERG K,CHAKRAVARTHY U,GERENDAS B S,et al. Guidelines for the management of diabetic macular edema by the European society of retina specialists(EURETINA)[J]. Ophthalmologica,2017,237(4):185-222.
[2] ZACCARDI F,ROCCA B,PITOCCO D,TANESE L,RIZZI A,GHIRLANDA G. Platelet mean volume,distribution width,and count in type 2 diabetes,im paired fasting glucose,and meta-bolic syndrome:a meta-analysis[J]. Diabetes Metab Res Rev,2015,31(4):402-410.
[3] ERGELEN M,UYAREL H. Plateletcrit:a novel prognostic marker for acute coronary syndrome[J]. Int J Cardiol,2014,177(1):161.
[4] EIBL N,KRUGLUGER W,STREIT G,SCHRATTBAUER K,HOPMEIER P,SCHERNTHANER G. Improved metabolic control decreases platelet activation markers in patients with type-2 diabetes[J]. Eur J Clin Invest,2004,34(3):205-209.
[5] BHAGAT N,GRIGORIAN R A,TUTELA A,ZARBIN M A. Diabetic macular edema:patho genesis and treatm ent[J]. Surv Ophthalm ol,2009,54(1):1-32.
[6] PRAIDOU A,PAPAKONSTANTINOU E,ANDROUDI S,GEORGIADIS N,KARAKIULAKIS G,DIMITRAKOS S. Vitreous and serum levels of vascular endothelial growth factor and platelet-derived growth factor and their correlation in patients with non-proliferative diabetic retinopathy and clinically significant macula oedema[J]. Acta Ophthalmol,2011,89(3):248-254.
[7] TETIKOGLU M,AKTAS S,SAGDIK H M,TASDEMIR YIGITOGLU S,ZCURA F. Mean platelet volume is associated with diabetic macular edema in patients with type-2 diabetes mellitus[J]. Semin Ophthalmol,2017,32(5):651-654.
[8]李海东,毛剑波,程丹,沈洁,沈丽君.2型糖尿病患者平均血小板体积与糖尿病黄斑水肿的关系[J].眼科新进展,2018,38(6):576-578.LI H D,MAO J B,CHENG D,SHEN J,SHEN L J. Correlation of mean platelet volume with diabetic macular edema in type2 diabetic patients[J]. Rec Adv Ophthalmol,2018,38(6):576-578.
[9] KANG J W,CHUNG H,KIM H. Correlation of optical coherence tomographic hyper-reflective foci with visual outcomes in different patients of diabetic macular edema[J]. Retina,2016,36(9):1630-1639.
[10]中华医学会眼科学会眼底病学组.我国糖尿病视网膜病变临床诊疗指南(2014年)[J].中华眼科杂志,2014,50(11):851-865.Chinese Ocular Fundus Diseases Society,Chinese Ophthalmological Society,Chinese Medical Association. Guidelines for clinical diagnosis and treatment of diabetic retino pathy in China[J]. Chin J Ophthalmol,2014,50(11):851-865.
[11] ACAN D,KARAHAN E,KOCAK N,KAYNAK S. Evaluation of systemic risk factors in different optical coherence to mographic patterns of diabetic macular edema[J]. Int J Ophthalmol,2018,11(7):1204-1209.
[12] GAUCHER D,SEBAH C,ERGINAY A,HAOUCHINE B,TADAYONI R,GAUDRIC A,et al. Optical coherence tomography features during the evolution of serous retinal detachment in patients with diabetic macular edema[J]. Am J Ophthalmol,2008,145(2):289-296.
[13] KIM B Y,SMITH S D,KAISER P K. Optical coherence tomographic patterns of diabetic macular edema[J]. Am J Ophthalmol,2006,142(3):405-412.
[14] GHOSH S,BANSAL P,SHEJAO H,HEGDE R,ROY D,BISWAS S. Correlation of morphological pattern of optical coherence tomography in diabetic macular edema with systemic risk factors in middle aged males[J]. Int Ophthalmol,2015,35(1):3-10.
[15] ALKURAYA H,KANGAVE D,ABU EL-ASRAR A M. The correlation between optical coherence to mographic features and severity of retino pathy,m acular thickness and visual acuity in diabetic macular edema[J]. Int Ophthalmol,2005,26(3):93-99.
[16] GASPARYAN A Y,AYVAZYAN L,MIKHAILIDIS D P,KITAS G D. Mean platelet volum e:a link between thrombosis and inflammation[J]. Curr Pharm Des,2011,17(1):47-58.
[17] KIM J H,BAE H Y,KIM S Y. Response:clinical marker of platelet hyperreactivity in diabetes mellitus[J]. Diabetes Metab J,2014,38(2):160-161.
[18] LIPPI G,SALVAGNO G L,NOUVENNE A,MESCHI T,BORGHI L,TARGHER G. The mean platelet volume is significantly associated with higher glycated hemoglobin in a large population of unselected out patients[J]. Prim Care Diabetes,2015,9(3):226-230.
[19] XIAO W,HUANG Y,DONG J,ZHANG X,HU J. Relationship between platelet volume indices with macro vascular and peripheral neuro pathy complications in type 2 diabetic patients[J]. J Diabetes,2014,6(4):298-303.
[20] KERNT M,THIELE S,LIEGL R G,KERNT B,EIBL K,HARITOGLOU C,et al. Axitinib modulates hypoxia-induced blood-retina barrier perm eability and expression of growth factors[J]. Growth Factors,2012,30(1):49-61.
[21] EHRLICH R,HARRIS A,CIULLA T A,KHERADIYA N,WINSTON D M,WIROSTKO B. Diabetic macular oedem a:physical,physiological and molecular factors contribute to this pathological process[J]. Acta Ophthalmol,2010,88(3):279-291.
[22] KIM M,LEE P,KIM Y,YU S Y,KWAK H W. Effect of intravitreal bevacizum ab based on optical coherence to mography patterns of diabetic macular edema[J]. Ophthalmologica,2011,226(3):138-144.
[23] KOYTAK A,ALTINISIK M,SOGUTLU SARI E,ARTUNAY O,UMURHAN AKKAN J C,TUNCER K. Effect of a single intravitreal bevacizum ab injection on different optical coherence to mographic patterns of diabetic macular oedem a[J].Eye(Lond),2013,27(6):716-721.
[24] GUPTA A,RAMAN R,KULOTHUNGAN V,SHARMA T. Association of systemic and ocular risk factors with neuro sensory retinal detachment in diabetic macular edem a:a case control study[J]. BMC Ophthalmol,2014,9:2-6.
[25] SHIMURA M,YASUDA K,YASUDA M,NAKAZAWA T. Visual outcome after Intraviteral bevacizum abdepends on the optical coherence to mographic patterns of patients with diffuse diabetic macular edema[J]. Retina,2013,33(4):740-747.


